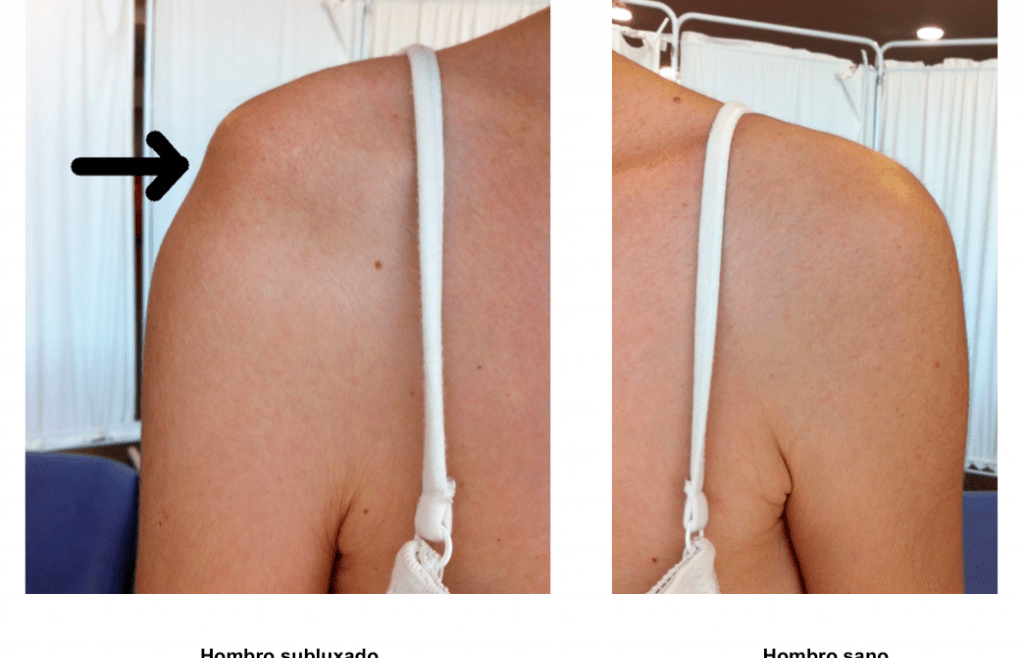
Muchas veces encontramos pacientes con ictus ya cronificados, donde tanto las sinergias como la debilidad de la musculatura extrínseca de la mano, generan posiciones y posibles deformidades en la muñeca, normalmente en posición de flexión.
Las restricciones en la extensión de muñeca, ya sean por problemas de estructuras blandas, como ligamento, tendón o sistema nervioso periférico, pueden ser tratadas a través de terapia manual.
El caso es que la necesidad de preparar la estructura para una actividad funcional, con vistas tanto al objetivo específico funcional, o hacia el aumento de «usabilidad» de la mano, puede ser una opción de tratamiento para reorientar la mano en el espacio, tal y como plantea el siguiente estudio:
«Manual mobilization of the wrist: A pilot study in rehabilitation of patients with a chronic hemiplegic hand post-stroke»
En este estudio realizaron movilizaciones postero-anteriores de la articulación del escafoides y semilunar con el radio, durante 30 minutos antes de las sesiones habituales (grupo control), 2 veces a la semana durante 6 semanas. Además, cabe destacar que esta movilización se usó durante tareas funcionales, lo que le da sentido a la orientación de la mano en su uso.
Se obtuvieron resultados interesantes en cuanto a la comparativa en ambos grupos en significación estadística, en la fuerza de agarre, en el rango pasivo de extensión de muñeca y finalmente, en el «Frenchay Arm Test» (tareas funcionales), con mejores resultados en el grupo experimental tras la terapia manual.
Esto nos hace reflexionar que la terapia manual, cada vez va adquiriendo no sólo un matiz pasivo, sino más bien activo dirigido hacia una tarea funcional, ya que la movilización de las estructuras tiende a ser dinámica y cambiante durante la ejecución de una tarea.
Además, la terapia manual enfocada hacia la tarea funcional favorece el uso de la extremidad y su correspondiente representación cortical, usualmente afectada por el problema persistente en los pacientes con ictus crónico, el «efecto no-uso o desuso».
Para más información, os dejamos el enlace del estudio.